

对于那些使用连续繁殖细胞的人来说,定期进行质量控制测试是绝对重要的。本文介绍了细胞系鉴定方法,这为细胞和细胞系特等细胞质控方面奠定了基础。
质量控制的基本步骤因构建的细胞资源类型而异。对于每个特定的细胞系,通常会用更广泛的表征基础来补充较少的描述性数据。而表征是细胞系许多特征的定义,其中一些特征可能是独一无二的,也可能用于具体识别或重新验证该细胞系。质量控制的基本步骤因构建的细胞资源类型而异。对于每个特定的细胞系,通常会用更广泛的表征基础来补充较少的描述性数据。细胞质量控制的基本步骤因构建的细胞资源类型而异。
一、什么是种子库
种子库的定义可能与用于功能抗体或其他生物制品生产等特定应用的定义不同。图 1 展示了种子库开发步骤的示意图。
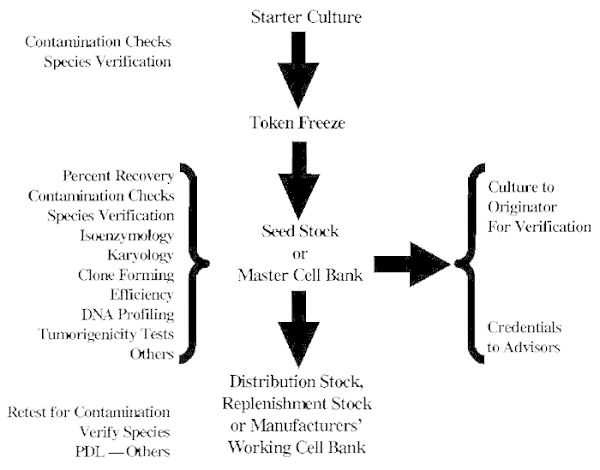
二 、微生物污染的防止
细胞培养系统中的微生物污染仍然是一个严重的问题。许多实验室都忽略了隐藏的污染物,甚至是容易分离的细菌和真菌。美国典型培养物保藏中心 (ATCC) 仍然接收含有酵母、丝状真菌和/或支原体污染物的培养物,即使是专利保藏中心。
A. 细菌和真菌
显微镜检查不足以检测严重污染;甚至其中一些也无法通过简单的观察轻易发现。因此,还需要进行一系列广泛的培养测试,以合理保证细胞系原液或培养基不含真菌和细菌。
B. 支原体感染
支原体对细胞培养物的污染可能比细菌或真菌的生长造成的污染更隐蔽。虽然某些支原体物种的存在可能由于诱导的退行性效应而明显存在,但其他支原体在培养物中代谢和增殖活跃,而不会在受污染的细胞系中产生任何明显的形态学变化。因此,与新陈代谢、表面受体、病毒-宿主相互作用等相关的细胞培养研究在对含有支原体的细胞系进行研究时,即使没有完全否定,也肯定会被怀疑解释。这些问题的严重性已通过来自测试服务和细胞培养库的已发布数据记录在案。目前也可以直接使用支原体清除试剂盒进行解决。
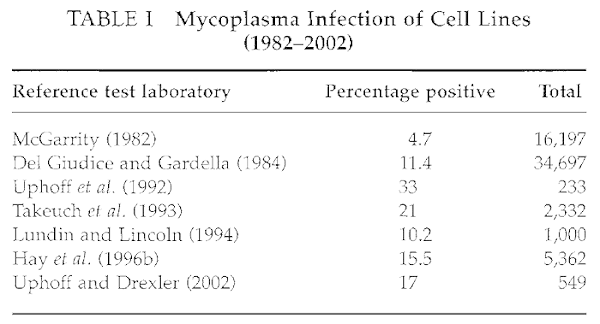
口腔支原体和其他人源支原体(人型支原体、M. salivarium 和 M. fermentas)是经常分离的支原体,这一 事实说明人类操作员会造成支原体污染的高发率。在 Del Giudice 和 Gardella (1984) 的研究中,在测试的 34,697 个品系中,3955 个(11%)呈阳性;这些分离株中有 36% 是人源性支原体。猪鼻支原体分离率很高,这可能是由于使用受污染的血清或在处理受感染生物制品的实验室中进行的培养物传播所致。经过近期的一项研究,提交给德国开发细胞库的
253 个细胞系中有 84 个 (33%) 感染了支原体。 1980 年以来发表的七个实验室的结果清楚地表明,支原体感染仍然是细胞培养领域中的一个非常主要的问题。大约 5% 到 20% 的培养物呈阳性。即使在今天,这也是范围。
细胞培养过程中如何减少支原体污染?
对于支原体污染主要可以通过以下方法来避免。通过有效实施方案来监测支原体细胞系。隔离所有新的、未经测试的生产线和使用机械移液辅助工具是其他的。大多数专家还强烈建议尽可能停止使用抗生素。无抗生素系统允许细菌和真菌过度生长,以便在无菌技术出现故障时提供现成的指示。当使用原代组织时,例如人类肿瘤样品,开始可以使用抗生素,但是在原代细胞群生长出来并冷冻保存后,可以在不含抗生素的培养基中进一步繁殖重组细胞。
三、病毒污染
确认细胞系中不存在病毒被认为是重要的问题。这些可能作为非细胞病变实体或以潜伏形式一起生存,增加了检测难度。明智的选择不仅对于选择可用于识别与细胞系相关的病毒的适当方法是必要的,而且对于识别违规物种也是必要的。小区资源的性质、其用户和可用预算,以及需要线路的预期目的,都会影响测试决策。
四、细胞交叉污染
无论细胞在培养物中生长在哪里,都存在无意添加和随后由另一个个体或物种的细胞过度生长的严重风险。不能仅依靠形态学标准来识别或鉴定细胞系。
在一项研究中,检查了来自 62 个实验室的 466 个品系。其中,有 75 个 (16%) 被发现被错误识别。有 43 个品系 (9%) 不是预期的物种,而 32 个品系 (7%) 要么是两个或多个品系的不正确混合,要么不是所述的单个品系
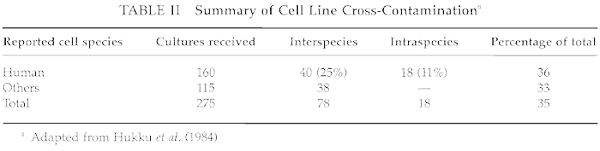
(Nelson-Rees, 1978)。Hukku等人. (1984) 在 18 个月的时间里检查了 275 行。他们的分析结果总结在表二中。有 96 条线 (35%) 与捐赠实验室所指示的不符。对于声称的人类系,36% 与预期不同,25% 是不同的物种,11% 是不同的人类个体。
为了降低细胞交叉污染的风险,培养技术人员需要层流罩以实现细胞培养操作。需要定期指导这些人在任何给定时间仅使用一种细胞系,每条细胞系使用一个培养基储液器,并避免将用于分配或混合细胞的移液器引入任何培养基储液器中。必须反复提醒技术人员用名称、通道和日期清楚地标记每个细胞培养物。不同颜色的标签可用于在扩增过程中更容易地将一种细胞系与另一种细胞系区分开来。
还必须指示技术人员在特定时间段内处理多条细胞系时,在打开紫外线灯和吹风机的情况下,留出至少
5 分钟的通风罩清理时间。在两次使用之间,应使用 70% 的乙醇擦拭每个头罩的内表面。
长期以来,核细胞学技术一直被用于监测细胞系之间的种间污染。在许多情况下,染色体的构成差异如此之大,以至于即使是粗略的显微镜观察也足够了。然而,细胞遗传学分析非常耗时,并且解释需要高度的技巧。核型是通过从显微照片中切割染色体并根据臂长、着丝粒位置、是否存在二次收缩等进行排列来构建的,这样只能使用自动分析系统来进行研究。
种内交叉污染
随着正在开发的细胞系数量的急剧增加,尤其是来自人体组织的细胞系,种内交叉污染的风险也相应增加。在需要使用当今可用的许多不同的人和鼠源细胞系的实验室中,这个问题尤为严重。
已经提到了使用酶迁移率研究来验证细胞系物种的方法。使用类似的技术,但使用不同的酶系统,人们还可以筛查种内细胞交叉污染。来自同一物种的不同个体的细胞系通常对给定的酶基因座显示不同的显性等位基因,其产物是多态的并且可通过电泳解析。在大多数情况下,这些等位基因酶(等位酶)的表型非常稳定。
应用重组 DNA 技术和克隆 DNA 探针来鉴定和定量等位基因多态性,为细胞系鉴定提供了额外的有力手段。这些多态性可以被认为是非常有用的标记,即使它们不是通过转录和翻译表达以产生结构酶促活性蛋白质。
已经为 DNA 分析应用(包括细胞系个体化)生产了针对高度可变的人类基因组区域的杂交探针。由于模式复杂,使用扫描设备也可以解释源自人类细胞系的概况。
另外,STR 基因座是基因组信息量较大的多态性标记之一。ATCC 使用的分析过程涉及在多重 PCR 反应(Promega PowerPlex 1.2 系统)中同时扩增八个 STR 位点和牙釉蛋白基因。
五、细胞系验证起源与作用
用于验证细胞系来源组织的标记可能与后生动物细胞的类型一样多。主要的演示方法包括精细结构分析、细胞骨架和组织特异性蛋白质的免疫学测试,当然还有针对组织细胞特定功能特性的极其广泛的生化测试。桥粒或 Weibel-Palade 体等超微结构特征分别识别上皮细胞和内皮细胞。使用单克隆抗体证明的中间丝蛋白的性质允许区分上皮亚型、间充质细胞和神经细胞。当试剂可靠且可用时,可以使用组织特异性和肿瘤特异性抗原。
苏州阿尔法生物联合海星生物可以为您提供细胞培养试剂、细胞株产品、细胞培养耗材、实验室仪器设备以及细胞检测技术服务 (细胞表面标记检测服务、细胞凋亡检测服务、细胞周期检测服务、细胞克隆形成率检测服务、细胞基因序列检测服务、细胞株支原体检测服务、细胞株STR分析服务、细胞染色体核型分析)等,还提供干细胞,多能干细胞,成骨诱导分化培养基,骨髓干细胞、胚胎干细胞、脐带血干细胞等细胞株、细胞系、细胞培养试剂、细胞培养耗材、细胞培养摇床、生物反应器、 实验室仪器、实验室设备、实验室消毒剂等,更多内容0512-62956104或18934597460进行了解