研究背景
· 近年来,由于超级毒力菌株的出现和广泛传播,CDI的全球负担有所加剧。艰难梭菌产生三种致病性相关的外毒素:毒素A( TcdA )、毒素B(TcdB)和艰难梭菌转移酶(CDT)。
· 在这三种毒素中,TcdB在引起胃肠道疾病中起着关键作用。TcdB是艰难梭菌的主要毒性因子,分为至少8个自然变种/亚型,其中1-4型与人类疾病相关。
· 第二群(clade 2)艰难梭菌,也称为超级毒力群,仅表达两种TcdB变种(TcdB2和TcdB4),这些变种不识别经典的Frizzled(FZD)受体。目前还不清楚这些TcdB变种如何靶向肠上皮细胞引发组织损伤。
研究思路
功能验证: 为了验证TFPI在体内是否是TcdB4的受体,研究人员使用了TFPI敲除的小鼠模型,并在小鼠结肠环扎模型中测试了TFPI对TcdB4介导的肠道损伤的保护作用。
策略的探索: 最后,研究人员探索了同时抑制TFPI和CSPG4两种受体结合位点的方法,以提供合适的TcdB保护效果。
研究结论
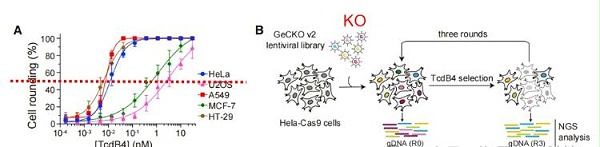
在HeLa细胞中进行了全基因组CRISPR-Cas9筛选,GeCKO v2向导RNA ( gRNA )文库并进行3轮TcdB4选择
2. NGS进行解码对识别的基因进行排序和绘图,标记出至少靶向三个gRNA的富集基因前30个。

细胞表面蛋白TFPI(组织因子途径抑制物): 是一种在人体内参与血液凝固调控的蛋白质。它主要存在于细胞膜上和细胞外空间 ,TFPI(组织因子途径抑制物)的不同形式,可能与毒素进入细胞的过程相关。
CSPG4、FZD1-2-7、TFPI: 这些都是细胞表面的蛋白质,与细胞对TcdB4的敏感性有关。
4. TcdB4对HeLa细胞的毒性机制通过和细胞表面结合发挥作用,膜蛋白TFPI和CSPG4正向调控,TFPI作用尤为明显。
PI-PLC: 磷脂酰肌醇特异性磷脂酶C(Phosphatidylinositol-specific Phospholipase C),是一种影响细胞信号传导的酶,,能够切割磷脂分子并释放GPI-锚定的蛋白质。
RAC1糖基化:指的是RAC1蛋白质的一种翻译后修饰,这里用作评估毒素作用的一个指标。
6. TFPIK1+K2(效应子)加量后可以使TcdB4侵染HeLa CSPG4/使细胞血红蛋白运输加快 ,且受 细胞膜表面CSPG4正向调控。
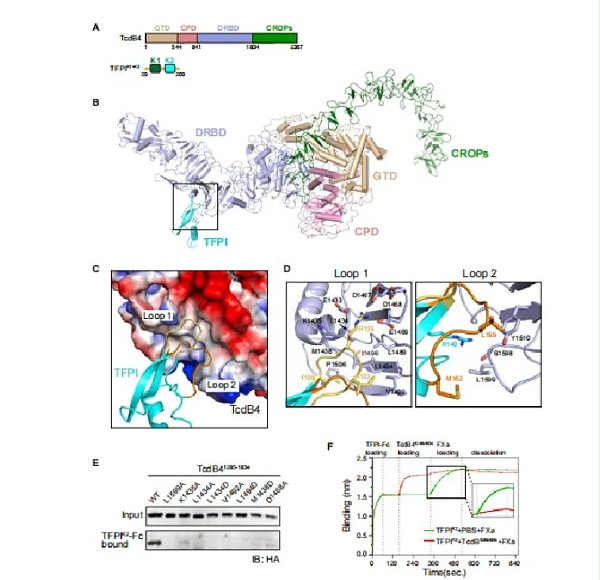
C 系统发育分析显示,TFPIK2的一级序列与TFPIK1的亲缘关系最为密切,相似性67.9%
7. TcdB4中L1599、K1435、L1434、V1492、L1494、M1438和D1468的点突变取消了TFPI结合能力,表明这些位置对受体识别很重要(TcdB4毒力因子识别位点)。