

标签:肿瘤 癌症 细胞质 癌细胞 肿瘤免疫 细胞免疫
人体内的每个细胞都含有大约 3 亿个双链 DNA 碱基对,这些双链 DNA 对整个细胞的一系列过程做出贡献,包括基因表达、代谢调节、组织特性和蛋白质生产。利用这一原理,激活cGAS-细胞质 DNA 传感器可以对抗癌症。
DNA 对细胞过程的深远影响可能让人难以相信它是通过一个细胞器:细胞核来完成其所有作用的。
事实上,细胞核外基因组 DNA 的存在通常表明存在问题。这可能意味着存在从入侵病毒带入的外来 DNA,或者发生了 DNA 损伤或细胞损伤。
虽然一段时间以来人们都知道细胞质 DNA 可以触发细胞防御以阻止病毒感染,即通过激活干扰素反应,但多年来,触发这种反应的细胞质 DNA 传感器仍然难以捉摸。
直到八年前,人们发现了一种新型的细胞质 DNA 传感器:环状 GMP-AMP 合酶,或 cGAS。
“詹姆斯” Chen博士和同事报告C气体的分离,它能够探测到细胞质DNA的能力,并激活信号级联。他们发现,在识别细胞质 DNA 后,cGAS 会产生环 GMP-AMP (cGAMP),然后激活干扰素基因刺激物 (STING)。额外的信号促进 I 型干扰素的表达,导致各种干扰素刺激基因的表达,随后激活免疫反应以对抗病毒。(见图1)
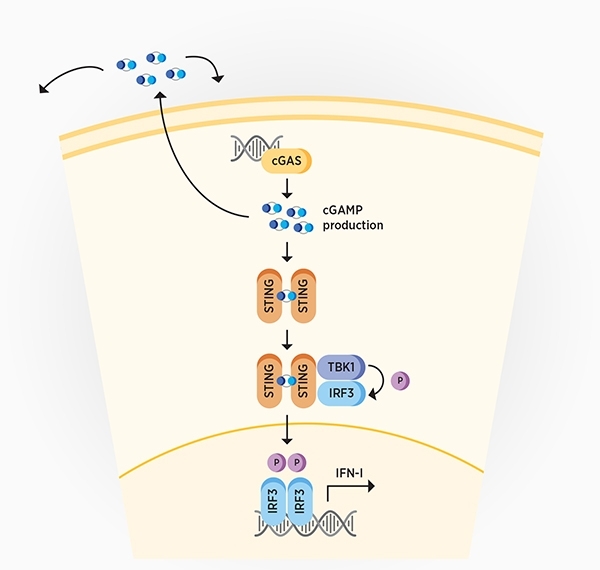
图 1: cGAS-STING 通路。检测到细胞质 DNA 后,cGAS 会产生 cGAMP,导致 STING 的二聚化和激活。STING 二聚体与 TBK1 结合,使 IRF3 磷酸化,导致其二聚化。Phospho-IRF3 二聚体易位至细胞核并促进 I 型干扰素的表达和随后的免疫信号传导。分泌的 cGAMP 激活周围细胞中的干扰素信号。
这一重大发现揭示了针对病毒和其他细胞质病原体的细胞防御机制的一个关键组成部分。不久之后,越来越多的研究证实 cGAS 可以识别各种病毒,并且某些病毒可以逃避或灭活cGAS 信号。
自 2013 年以来,cGAS-STING 通路在病毒感染背景之外的作用也变得很明显,有助于细胞衰老、炎症,甚至抗肿瘤免疫。与病毒类似,癌症可以克服或利用这种免疫激活途径的组成部分,提供各种治疗机会。在这里,我们回顾了关于癌细胞与 cGAS-STING 通路之间相互作用的最新研究。
CGAS 激活促进抗肿瘤免疫
最近的研究揭示了 cGAS 如何在癌细胞中被激活。今年早些时候发表在Cancer Cell 上的两项研究检查了错配修复缺陷 (dMMR) 癌症中抗肿瘤免疫的激活。一项研究发现,错配修复中的缺陷导致 DNA 断裂处的 DNA 过度消化;这导致染色体不稳定,受损的 DNA 输出到细胞质中,以及 cGAS-STING 通路的激活。在伴随的研究中研究人员确定,dMMR 细胞中 cGAS 的这种激活会刺激干扰素反应,促进抗肿瘤免疫,并增强对免疫检查点抑制的反应。与这些临床前发现一致,研究人员观察到,肿瘤微卫星不稳定性高(与 dMMR 相关)和 cGAS 水平低的患者生存率较差。总之,这些结果突出了 cGAS-STING 通路在刺激抗肿瘤免疫中的作用,并表明免疫检查点抑制剂在 dMMR 肿瘤中的有效性可能部分归因于 cGAS 的激活。
除了激活内在和先天免疫途径外,cGAS 检测细胞质 DNA 还可以触发适应性免疫的刺激。在AACR 2021年会的一次演讲中,Chen 的研究小组在 2013 年发现了 cGAS,他解释说,被树突细胞捕获的癌细胞会将 DNA 和 cGAMP 释放到树突细胞的细胞质中。这不仅会刺激 STING 和下游干扰素信号,还会激活树突状细胞,然后将肿瘤相关抗原传递到淋巴结,导致肿瘤特异性 T 细胞的释放。
癌细胞反击
cGAS-STING 通路激活免疫反应对癌症来说可能是灾难性的,因为免疫系统的组成部分可以靶向并破坏恶性细胞。毫不奇怪,许多癌症已经进化出克服、逃避或利用 cGAS 介导的抗肿瘤免疫的机制。(见图 2,红色)
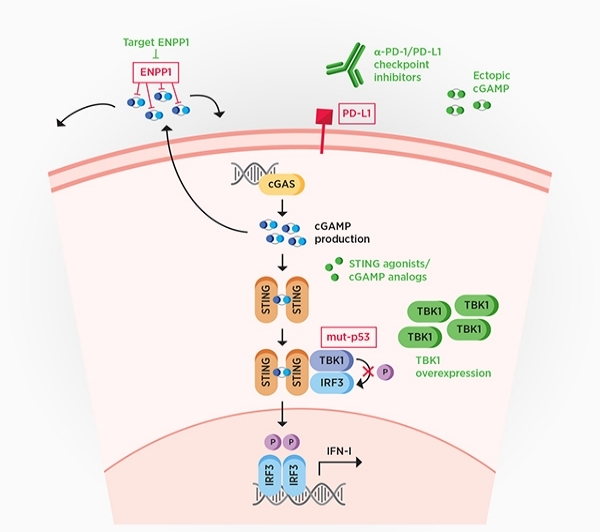 图 2: 癌症与 cGAS-STING 通路之间的相互作用。红色显示的是癌细胞用来克服、逃避或利用 cGAS-STING 通路的机制,例如降解 cGAMP、表达 PD-L1 免疫检查点蛋白和抑制 TBK1。潜在的治疗机会以绿色表示。
图 2: 癌症与 cGAS-STING 通路之间的相互作用。红色显示的是癌细胞用来克服、逃避或利用 cGAS-STING 通路的机制,例如降解 cGAMP、表达 PD-L1 免疫检查点蛋白和抑制 TBK1。潜在的治疗机会以绿色表示。
根据最近发表在AACR 期刊Cancer Discovery上的一项研究,一些癌细胞通过降解细胞外 cGAMP 来逃避抗肿瘤免疫。细胞外 cGAMP 的降解阻止了相邻细胞中的免疫信号传导,并且还会产生免疫抑制性腺苷作为副产物。该研究表明,ENPP1 外核苷酸酶负责细胞外 cGAMP 的分解,并且该酶在高度转移的癌细胞中上调。细胞外而非细胞内 cGAMP 的选择性靶向可能允许癌细胞逃避由细胞外 cGAMP 诱导的抗肿瘤免疫,同时利用 细胞内 cGAMP 的某些促进转移特性。
癌细胞破坏 cGAS 介导的抗肿瘤免疫的另一种策略是抑制干扰素刺激基因的表达。今年早些时候在Cancer Cell 上发表的一项研究发现,存在于大部分癌症中的突变 p53 与 STING 下游的蛋白质 TANK 结合激酶 1 (TBK1) 结合。这可以防止 TBK1 磷酸化和激活干扰素调节因子 3 (IRF3),后者在激活时通常会介导 I 型干扰素基因的转录。通过这种方式,p53 突变的癌症能够破坏 cGAS 介导的抗肿瘤免疫。
根据陈在AACR年会上的讲话,除了破坏先天免疫外,癌细胞还可以通过上调免疫检查点蛋白PD-L1来逃避cGAS介导的适应性免疫,从而逃避活化的T细胞。
调节 CGAS-STING 通路用于癌症治疗
癌细胞与 cGAS-STING 通路之间的相互作用提供了各种治疗机会。(参见图 2,绿色)例如,靶向癌症中的 ENPP1 外核苷酸酶可以恢复旁分泌免疫信号,并可以防止产生免疫抑制性腺苷。临床前实验表明,ENPP1 缺失可抑制转移,恢复肿瘤中的免疫细胞浸润,并促进对免疫检查点抑制剂的反应。正在 开发的腺苷拮抗剂也可用于减少免疫抑制策略。
另一种潜在的治疗方法是在 p53 突变的癌症中过度表达 TBK1。为支持这种方法,临床前实验发现过表达 TBK1 足以绕过突变 p53 的免疫抑制作用并恢复干扰素刺激的基因表达、免疫细胞功能和癌细胞的靶向。
此外,cGAS-STING 通路的组成部分可用作生物标志物来预测对癌症治疗的临床反应。已显示低 cGAS 水平与接受免疫检查点抑制剂的患者的存活率降低有关,并且 发现ENPP1 表达与对这种免疫疗法的抵抗相关。
操纵 cGAS-STING 通路也可以改善对现有癌症疗法的反应。发表在 AACR 杂志《血液癌症发现》上的一项临床前研究发现,STING 激动剂增强了硼替佐米诱导的免疫原性细胞死亡,硼替佐米是一种用于治疗多发性骨髓瘤的蛋白酶体抑制剂。虽然还需要更多的研究,但该研究的结果表明,硼替佐米和 STING 激动剂的联合治疗可以使多发性骨髓瘤患者受益。STING 激活——通过 STING 激动剂或异位 cGAMP 治疗——也已被证明可以增强各种破坏 DNA 的癌症疗法的效果,包括 放射、化学疗法和PARP 抑制剂。
Chen 在今年 AACR 年会上提供的数据表明,激活 cGAS-STING 通路也可能改善对免疫检查点抑制的反应。Chen 及其同事先前观察到 cGAS 是免疫检查点抑制的抗肿瘤作用所必需的。在年会上发表的研究中,他们发现作为 STING 激动剂的研究性 cGAMP 类似物在癌症小鼠模型中以剂量依赖性方式与抗 PD-L1 免疫检查点抑制剂协同作用。联合治疗抑制了转移并使抗 PD-L1 耐药细胞对免疫检查点抑制敏感。此外,用 cGAMP 类似物治疗导致与免疫原性肿瘤微环境相关的趋化因子的释放。基于这些结果,一个 已启动I 期临床试验,以在各种癌症类型的患者中单独评估研究性 cGAMP 类似物或与免疫检查点抑制联合使用。
距离 cGAS 的关键发现还不到 10 年。在这短短的时间内,这种细胞质 DNA 传感器的已知作用已远远超出抗病毒防御,扩展到细胞衰老和抗肿瘤免疫等重要功能。
更多 cGAS相关问题,请点击苏州阿尔法生物实验器材有限公司 进入官网或0512-62956104联系。
------摘自《ACCR杂志》